Аденокарцинома протоков поджелудочной железы (PDAC) — смертельное заболевание, которое, по прогнозам, к 2030 году станет второй по значимости причиной смертности от рака в США после канцера легких и бронхов с 63000 тыс смертей в год.1 Одной из причин подобного мрачного прогноза является поздняя диагностика опухолей (в 90% случаев) после их распространения за пределы поджелудочной железы с системными метастазами в у более половины пациентов.2,3 Это подчеркивает необходимость в инструментах для обнаружения PDAC до момента ее распространения за пределы железы, а также в методах лечения, которые более эффективно эрадицируют PDAC клетки после их метастазирования. За последнее десятилетие фундаментальные и трансляционные исследования значительно улучшили наше понимание биологических процессов, которые управляют панкреатическим туморогенезом, и это понимание начинает использоваться для улучшения лечения пациентов с раком поджелудочной железы.
Патогенез рака поджелудочной железы
Патология неоплазии поджелудочной железы
PDAC возникает из неинвазивных предраковых поражений, которые курабельны в случае их ранней детекции и лечения (Фиг. 1). Эти предраковые поражения классифицируются согласно размеру и вовлечению протоков поджелудочной железы. Большинство PDAC является результатом микроскопической интраэпителиальной неоплазии поджелудочной железы (PanIN), неоплазмы, вовлекающей протоки поджелудочной железы, размер которой согласно определению <5 мм. Гораздо меньшая часть PDAC (<10%) возникает в результате внутрипротоковых папиллярных муцинозных новообразований (IPMN), макрокистозных поражений, которые вовлекают протоковую систему поджелудочной железы.4–6 Наименее распространенная предраковая неоплазма, муцинозная кистозная неоплазма, клинически и патологически отличается. Муцинозные кистозные неоплазмы не включают протоковую систему и имеют характерную строму овариального типа. Они гораздо чаще встречаются у женщин и поражают тело/хвост поджелудочной железы.7 Уникальные патологические черты каждого поражения приводят к различным клиническим вызовам. Например, вследствие своего большего размера IPMN обычно выявляются случайно при визуализационных исследованиях брюшной полости, что требует определенных подходов к наблюдению и вмешательству у этих пациентов.8 Напротив, PanIN редко детектируется случайно. Хотя патологические черты этих предраков хорошо изучены, сохраняется дискуссия относительно клеток происхождения рака поджелудочной железы. Анатомическое расположение предраков в протоковой системе поддерживает протоковые клетки происхождения, но исследования на мышиных моделях демонстрируют, что ацинарные клетки могут вызывать PanIN после повреждения и метаплазии поджелудочной железы. Однако сложно подтвердить подобные результаты на образцах человека.
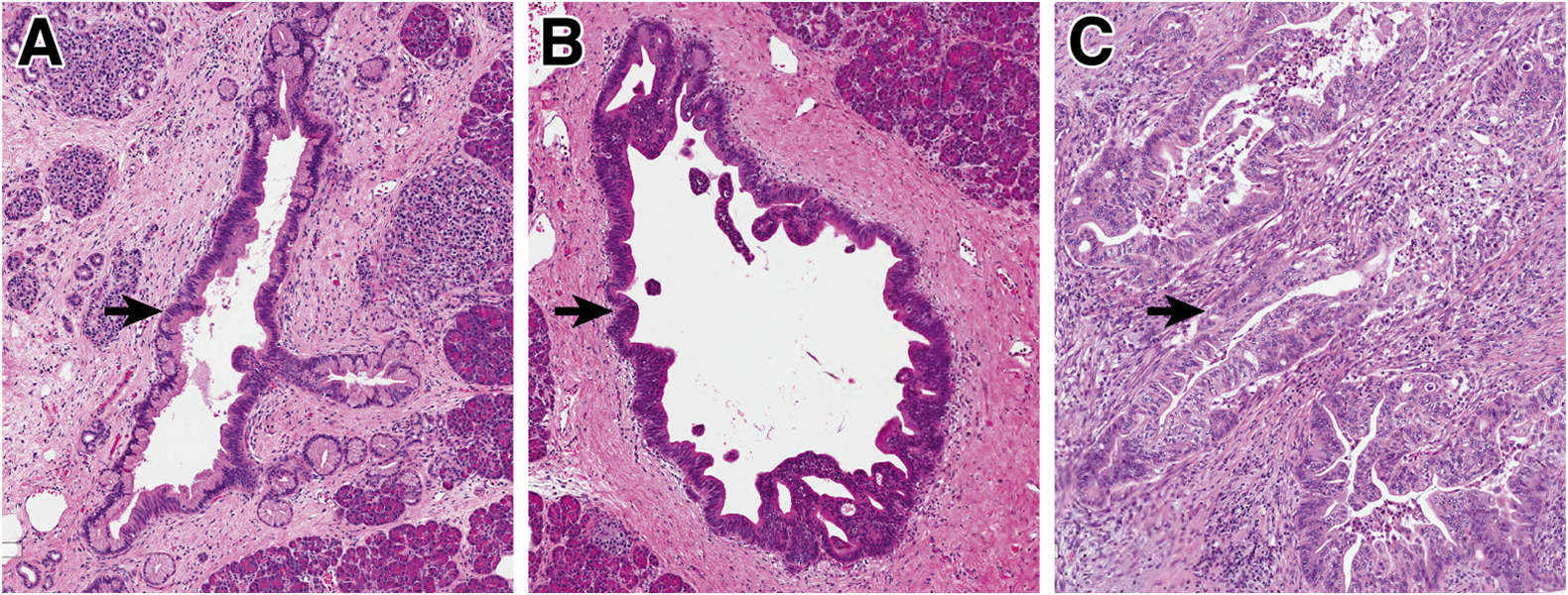
Фиг. 1. Предраковая неоплазия поджелудочной железы. Низкозлокачественная PanIN вовлекает протоки поджелудочной железы. Она имеет апикальный муцин и легкую цитологическую атипию, при этом ядра по-прежнему сохраняют свою полярность. (B) Высокозлокачественная PanIN демонстрирует усиление архитектурной и цитологической атипии, включающей архитектурную сложность, ядерный плеоморфизм и потерю ядерной полярности. (C) Инвазивная PDAC демонстрирует сильную архитектурную и цитологическую атипию с высоким десмопластическим ответом в строме
Предраковые новообразования поджелудочной железы чрезвычайно распространены, и их распространенность нарастает с возрастом; например, одно аутопсийное исследование пожилых людей выявило PanIN в >75% полностью забранных образцов поджелудочной железы.10,11 Хотя эти поражения имеют риск прогрессирования в PDAC, большинство из них не перерастают в рак, и сами по себе они не имеют риск распространения за пределы поджелудочной железы.12,13 Морфологически эти поражения классифицируются как низкозлокачественные или высокозлокачественные на основании архитектурной и цитологической атипии (рис. 1).4 Эта двухуровневая градирующая система (низкозлокачественная vs высокозлокачественная) представляет ревизию ранее использовавшейся трехуровневой градацирующей системы предканцеров поджелудочной железы; переход на двухуровневую систему обусловлен повышенной воспроизводимостью между наблюдателями, а также клинической эффективностью пересмотренной системы. Низкозлокачественные предраки имеют базально ориентированные ядра и цитологическую легкую-умеренную атипию (рис. 1А), а высокозлокачественные предраки имеют выраженные архитектурные альтерации (крибриформные, микроспапиллярные, отпочковывающиеся), утрату ядерной полярности и сильную цитологическую атипию (Фиг. 1B).4
————
————